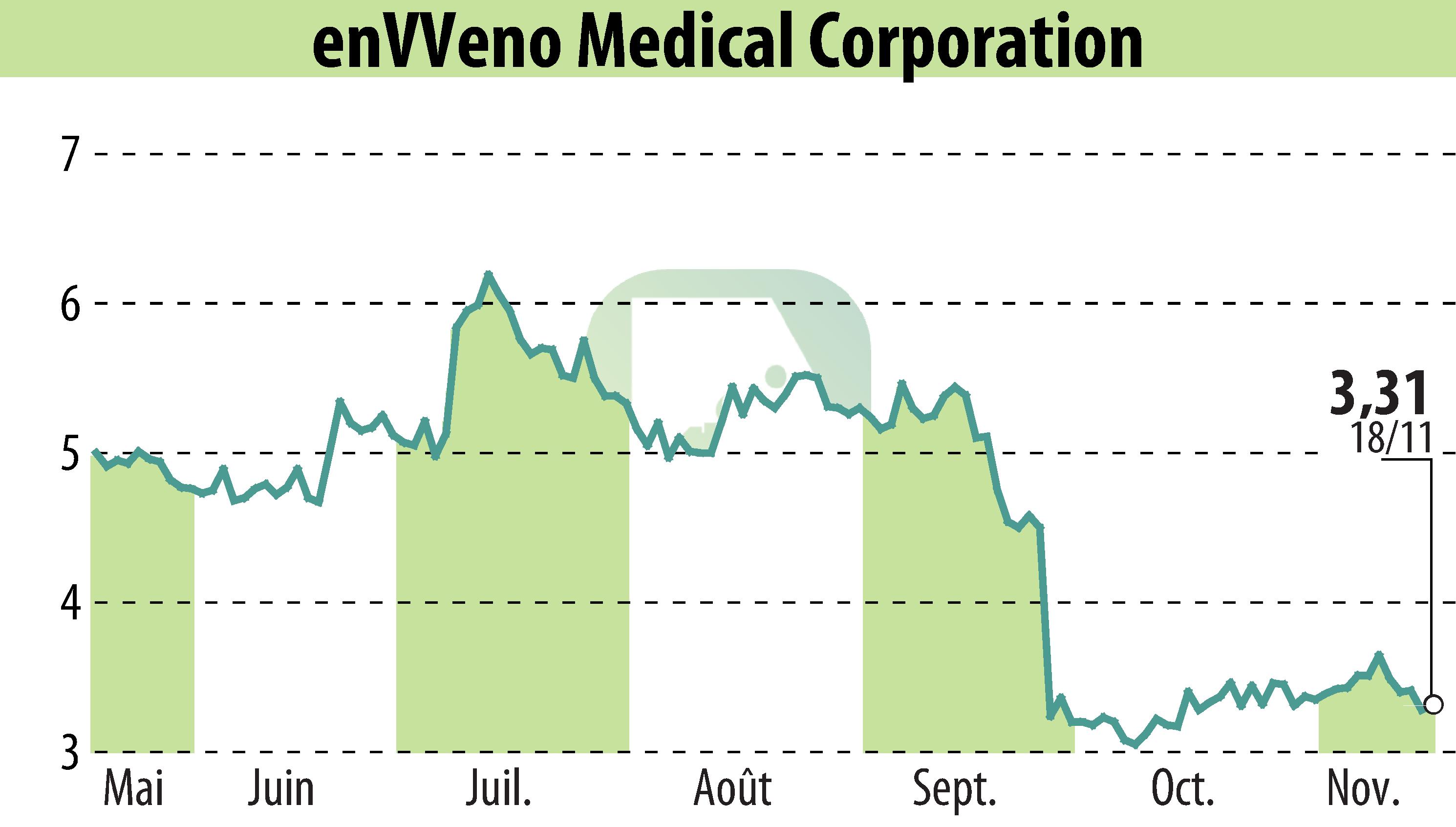
on EnVVeno Medical Corporation (NASDAQ:NVNO)
EnVVeno Medical demande l'approbation de la FDA pour VenoValve
enVVeno Medical Corporation a soumis le dernier module de sa demande d'approbation préalable à la mise sur le marché (PMA) à la FDA américaine pour obtenir l'approbation de la VenoValve. Cette demande est essentielle pour les projets de la société visant à commercialiser et à vendre le dispositif aux États-Unis. La demande comprend cinq modules, dont quatre ont été approuvés. Le dernier module comprend les données cliniques de l'essai pivot SAVVE et les informations d'étiquetage proposées.
La VenoValve est destinée au traitement de l'insuffisance veineuse chronique (IVC) sévère causée par une thrombose veineuse profonde. Cette pathologie affecte la vie quotidienne et peut entraîner des symptômes graves tels que des ulcères veineux. En l'absence de traitement efficace contre l'IVC veineuse profonde, enVVeno estime qu'il existe un marché potentiel de 2,5 millions de candidats par an aux États-Unis
En outre, la société développe une valve non chirurgicale de nouvelle génération, dont les essais devraient commencer en 2025. Les données définitives à l'appui du PMA de VenoValve seront présentées lors du symposium VEITH.
R. P.
Copyright © 2025 FinanzWire, all reproduction and representation rights reserved.
Disclaimer: although drawn from the best sources, the information and analyzes disseminated by FinanzWire are provided for informational purposes only and in no way constitute an incentive to take a position on the financial markets.
Click here to consult the press release on which this article is based
See all EnVVeno Medical Corporation news
